Terpenoid merupakan bentuk senyawa dengan keragaman struktur yang besar
dalam produk alami yang diturunkan dari unit isoprena (C5) yang bergandengan
dalam model kepala ke ekor (head-to-tail), sedangkan unit isoprena
diturunkan dari metabolisme asam asetat oleh jalur asam mevalonat (mevalonic
acid : MVA). Adapun reaksinya adalah sebagai berikut (Anonim, 2006).
Senyawa ini memiliki gugus hidroksi pada atom C21 dengan titik lelehnya
265_-266_C, dan dari berat molekul 440, rumus molekul yang diduga adalah
C30H48O2.
Berdasarkan klasifikasi terpenoid, sebagian besar terpenoid mengandung
atom karbon yang jumlahnya merupakan kelipatan lima. Penyelidikan kimia
selanjutnya menunjukkan bahwa sebagian besar terpenoid mempunyai kerangka
karbon yang dibangun oleh dua atau lebih unit C-5 ini dinamakan karena kerangka
karbonnya sama seperti isopren.
Penyelidikan yang lebih seksama lagi mengenai struktur molekul terpenoid
telah mengungkapkan bagaimana unit-unit isoprene tersebut saling berkaitan
secara teratur, dimana “kepala” dari unit yang satu berkaitan dengan “ekor”
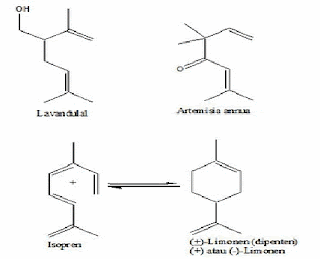
dari unit lain. Cara penggabungan “kepala ke ekor” dari unit-unit isoprene
dapat dilihat pada gambar dibawah ini.
Pada gambar diatas dapat dijelaskan bahwa kaidah ini merupakan cirri
khas dari sebagian besar terpenoid sehingga dapat digunakan sebagai hipotesa
dalam menentukan struktur terpenoid. Tetapi pada beberapa monoterpen tidak
mengikuti kaidah isoprene.
Sebagian besar terpenoid mempunyai kerangka karbon yang dibangun oleh
dua atau lebih unit C-5 yang disebut isopren. Klasifikasi terpenoid ditentukan
dari unit isopren atau unit C-5 penyusun senyawa tersebut. Senyawa umum
biosintesa terpenoid dengan terjadinya 3 reaksi dasar, yaitu:
- Pembentukan isoprene aktif berasal dari asam asetat melalui asam mevalonat.
- Penggabungan senyawa dan ekor dua unit isopren akan membentuk mono-, seskui-, di-, sester-, dan poli-terpenoid.
- Pengabungan ekor dan ekor dari unit C15 atau C20 menghasilkan terpenoid atau steroid.
Senyawa terpenoid dapat dikelompokkan sebagai
berikut :
Nama
|
Rumus
|
Sumber
|
Monoterpen
|
C10H16
|
Minyak
Atsiri
|
Seskuiterpen
|
C15H24
|
Minyak
Atsiri
|
Diterpen
|
C20H32
|
Resin
Pinus
|
Triterpen
|
C30H48
|
Saponin,
Damar
|
Tetraterpen
|
C40H64
|
Pigmen,
Karoten
|
Politerpen
|
(C5H8)n
n 8
|
Karet Alam
|
Monoterpeoid
merupakan senyawa essence dan memiliki dan memiliki bau yang spesifik
yang dibangun oleh 2 unti isopren atau dengan jumlah atom karbon 10. Lebih dari
1000 jenis senyawa monoterpenoid telah diisolasi dari tumbuhan tingkat tinggi,
binatang laut, serangga, dan jenis vertebrata dan struktur senyawanya telah
diketahui.
Struktur
dari senyawa monoterpenoid yang telah dikenal merupakan perbedaan dari 38 jenis
kerangka yang berbeda, sedangkan prinsip dasar penyusunannya tetap sebagai
penggabungan kepala dan ekor dari 2 unit isoprene. Struktur monoterpenoid dapat
berupa rantai terbuka dan tertutup atau siklik. Senyawa monoterpenoid banyak
dimanfaatkan sebagai antiseptik,
ekspektoran, spasmolotik, dan sedatif. Disamping itu monoterpenoid yang sudah
banyak dikenal banyak dimanfaatkan sebagai bahan pemberi aroma makanan dan
parfum dan ini banyak digunakan komersial dalam perdagangan.
Dari segi
biogenetik, perubahan geraniol nerol dan linaol dari salah satu menjadi yang
lain berlangsung sebagai akibat reaksi isomerisasi. Ketiga alkohol ini yang berasal
dari hidrolisa geranil pirofosfat (GPP) dapat menjadi reaksi-reaksi sekunder,
misalnya dehidrasi menghasilkan mirsen, oksidasi menghasilkan sitral dan
oksidasi reduksi menghasilkan sitronelal.
Peubahan GPP
in vivo menjadi senyawa-senyawa monoterpen siklik dari segi biogenetic
disebabkan reaksi siklisasi yang diikuti oleh reaksi-reaksi sekunder. Senyawa
seperti monoterpenoid mempunyai kerangka karbon yang banyak variasinya. Oleh
karena itu penetapan struktur merupakan hal yang penting. Jenis kerangka karbon
monoterpenoid antara lain dapat ditetapkan oleh reaksi dehidrogenasi menjadi
senyawa aromatik. Penetapan struktur selanjutnya adalah melalui penetapan gugus
fungsi dari senyawa yang bersangkutan.
Seskuiterpen
Seskuiterpenoid
merupakan senyawa terpenoid yang dibangun oleh 3 unit isoprene yang terdiri
dari kerangka unit asiklik atau bisiklik dengan kerangka naphtalen. Senyawa
terpenoid mempunyai boiaktifitas yang cukup besar, diantaranya sebagai
antifeedant, hormone, antimikroba, antibiotic dan toksin sebagai regulator
pertumbuhan tanaman dan pemanis.
Senyawa-senyawa
seskuiterpen diturunkan dari cis-farnesil pirofosfat dan trans farnesil
piropospat melaului reaksi siklisasi dan reaksi sekunder lain. Kedua isomer
farnesil piropospat ini dihasilkan dari melalui mekanisme yang sama seperti
isomerisasi abtara geranil dan nerol.
Diterpenoid
merupakan senyawa yang mempunyai 20 atom karbon yang dibangun oleh 4 unti
isoprene. Senyawa ini mempunyai bioaktifitas yang cukup luas yaitu sebagai
hormone pertumbuhan tanaman, podolakton inhibitor pertumbuhan tanaman,
antifeedant serangga, inhibitor tumor, senyawa pemanis, abtifouling dan anti
karsinogenik. Senyawa diterpenoid dapat membentuk asiklik, bisiklik, trisiklik,
dan tetrasiklik. Tata nama yang digunakan merupakan tata nama trivial.
Terpenoid
tidak teratur
HUBUNGAN
STRUKTUR DAN KEREAKTIFAN TERPENOID DARI RIMPANG JAHE TERHADAP PENYAKIT
SERANGAN JANTUNG DAN STROKE
Terpenoid
merupakan komponen penyusun minyak atsiri. Terpenoid secara luas tersebar
di alam, sebagian besar ditemukan di tumbuhan tingkat tinggi. Terpenoid terdiri
atas beberapa senyawa antara lain minyak atsiri yang tersusun atas
monoterpenoid, seskuiterpenoid yang mudah menguap; Triterpenoid yang sukar
menguap; Triterpenoid dan steroid yang tidak menguap dan pigmen karetonoid.
Jahe adalah tanaman rimpang yang sangat populer
sebagai rempah-rempah dan bahan obat. Rimpangnya berbentuk jemari yang menggembung
di ruas-ruas tengah. Rasa dominan pedas disebabkan senyawa keton bernama
zingeron. Selain zingeron, juga ada senyawa oleoresin (gingerol, shogaol),
senyawa paradol yang turut menyumbang rasa.
Jahe merupakan rimpang dari tanaman bernama ilmiah Zingiber Officinale Roscoe.
Jahe merupakan rimpang dari tanaman bernama ilmiah Zingiber Officinale Roscoe.
Jahe sering kita temui sehari-hari. Banyak manfaat
yang kita dapat dari penggunaan jahe. Diantaranya sebagai bumbu masak, pemberi
aroma, dan rasa pada roti, kue, biscuit, kembang gula, serta berbagai minuman
(bandrek, sekoteng, dan sirup). Jahe juga dapat digunakan pada obat tradisional
sebagai obat sakit kepala, obat batuk, masuk angin,untuk mengobati gangguan
pada saluran pencernaan, stimulansia, diuretik, rematik, menghilangkan rasa
sakit, obat antimual dan mabuk perjalanan, karminatif (mengeluarkan gas dari
perut), kolera, diare, sakit tenggorokan, difteria, neuropati, sebagai penawar
racun ular dan sebagai obat luar untuk mengobati gatal digigit serangga,
keseleo, bengkak serta memar. Kandungan senyawa dalam jahe ada 2 golongan
senyawa berdasarkan kemudahan menguap, yaitu golongan senyawa volatil (mudah
menguap) dan golongan non-volatil. Senyawa yang menyebabkan pedas diatas
merupakan senyawa non-volatil.
Jika kita menumbuk seruas jahe, maka akan timbul
aroma khas yang kuat, dan jika kita hirup akan memberi suasana hangat di hidung
kita. Aroma khas ini berasal dari minyak atsiri yang terkandung didalamnya.
Minyak astiri merupakan senyawa volatil atau mudah menguap, sehingga baunya
tercium oleh hidung kita. Minyak ini juga menyebabkan rasa jahe yang khas.
Minyak atsiri dalam jahe merupakan gabungan dari senyawa terpenoid yang terdiri dari senyawa-senyawa
seskuiterpena, zingiberena, bisabolena, sineol, sitral, zingiberal (ada yang
menyebut zingiberol, tapi keduanya adalah senyawa berbeda; zingiberal
mengandung gugus aldehid, sedangkan zingiberol mengandung gugus
hidroksida,-OH), felandren (phellandrena),borneol, sitronellol, geranial,
linalool, limonene, kamfena. Minyak atsiri yang terkandung dalam jahe antara 1
sampai 3 %. Jahe menghambat agregasi platelet sehingga dapat mencegah serangan
jantung dan stroke (Srivastava, et al, 1964). Pemberian jahe terhadap pasien
dengan penyakit arteri koroner menyebabkan pasien tersebut menghasilkan
penurunan dalam agregasi platelet (Bordia, A, 1997). Tingginya kandungan mineral
ini dalam jahe membuat jahe cocok sebagai obat kejang otot, depresi,
hipertensi, lemah otot, kebingungan, perubahan kepribadian, mual, kekurangan
koordinasi dan penyakit gastrointestinal. Tingginya kandungan potassium dalam
jahe akan melindungi tubuh dari kedinginan, kelumpuhan, sterilitas, kelemahan
otot, lesu mental, kebingungan, kerusakan ginjal dan kerusakan hati.
PERMASALAHAN:
- Pada gambar diatas dapat dijelaskan bahwa kaidah ini merupakan ciri khas dari sebagian besar terpenoid sehingga dapat digunakan sebagai hipotesa dalam menentukan struktur terpenoid. Tetapi pada beberapa monoterpen tidak mengikuti kaidah isoprene. jelaskan monoterpenoid yang mana yang tidak mengikuti kaidah terpenoid ? dan Apa alasan senyawa tersebut tidak mengikutinya ?
- Pada artikel di atas dikatakan bahwa bagian gugus dari senyawa terpenoid pada jahe dapat menjadi obat untuk menurunkan agregasi platelet sehingga dapat mencegah serangan jantung dan stroke. Yang menjadi permasalahan saya, bagaimana keterkaitan struktur dan kereaktifan dari terpenoid tersebut sehingga dapat mempengaruhi penurunan agregasi platelet?